Vorhofflimmern - wann hilft die Katheterbehandlung?
Die Katheterbehandlung (Katheterablation) ist eine bewährte Behandlungsmöglichkeit von Vorhofflimmern mit dem Ziel den Herzrhythmus zu kontrollieren.1 Eine Rhythmuskontrolle kann durch verschiedene Medikamente, effizienter jedoch mittels der Katheterablation erreicht werden. Der größte klinische Nutzen dabei ist die dauerhafte Reduktion Arrhythmie-bedingter Beschwerden.2 Bei ausgewählten Patientengruppen lässt sich daneben auch eine Reduktion der Sterblichkeitsrate erzielen.3,4
Wann ist eine Katheter-gestützte Rhythmusbehandlung (Ablation) von Vorhofflimmern sinnvoll?
Vorhofflimmern ist die häufigste anhaltende Rhythmusstörung, an der in etwa 10 Millionen Europäer leiden. Sie lässt das individuelle Risiko für Komplikationen wie Schlaganfälle und Herzinsuffizienz deutlich steigen. Häufige Krankenhausaufenthalte und Einschränkung der Lebensqualität mit verminderter Belastbarkeit, Luftnot, dem Gefühl von Herzrasen, Schwindel, etc.) sind nur einige der vielen unangenehmen Folgen. Aus diesem Grund empfiehlt die Europäische Gesellschaft für Kardiologie gerade bei Patient:innen, die Symptome verspüren, eine Kontrolle des Herzrhythmus anzustreben.2 Voraussetzung dafür sind allerdings auch die Bereitschaft der Patient:innen, eine Blutverdünnung einzunehmen, sowie gewisse messwerte in der Herzultraschalluntersuchung. Weiters sollte das Vorhofflimmern nur vorübergehend (intermittierend) auftreten, oder wenn es dauerhaft auftritt, nicht länger als 12 Monate bestehen.
Die Katheterablation (Verödung) von Vorhofflimmern
Vorhofflimmern entsteht meist in den Lungenvenen, welche in den linken Herzvorhof münden (Abb. 1). Das Ziel bei der Katheterablation ist es das auslösende Gebiet in den Lungenvenen von den Herzmuskelzellen elektrisch zu isolieren. Das kann durch eine Verödungslinie um die Venen herum erreicht werden. Es gibt mehrere Methoden, um Lungenvenen zu isolieren, die sich verschiedener Energieformen bedienen. So kann man sowohl mittels Wärme- (Abb. 2a), als auch Kälteenergie die Stromleitfähigkeit von Herzmuskelzellen beeinflussen. Eine neue Methode bedient sich schnell applizierter, starker elektrischer Impulse (Pulsed Field Ablation = PFA, Abb. 3), die das elektrische Feld der Herzmuskelzelle stören und so zu einer elektrischen Isolierung führen, ohne Kälte- oder Wärmeenergie zu benötigen.
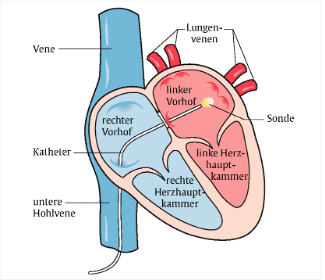
Abbildung 1: Schematische Darstellung der Herzhöhlen. Man sieht die Schleuse, welche über die Leistenvene ihren weiteren Weg über die große untere Hohlvene in den rechten Vorhof findet. Um in den linken Vorhof zu gelangen, muss dann die Scheidewand punktiert werden
Abbildung 2a: Kontinuierliches Temperaturmonitoring (dünner Pfeil) und Messung des Anpressdrucks (dicker Pfeil) während der Ablation, in grau: Anatomisches Map (=Zeichnung) des linken Herzvorhofs, Ablationskatheter im Zentrum, die roten Punkte entsprechen den Verödungspunkten.
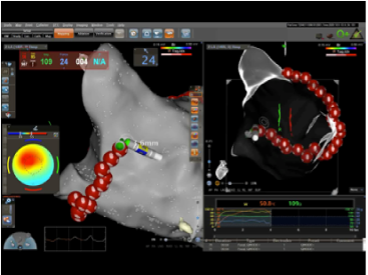
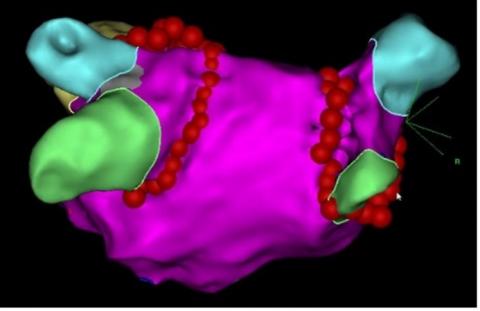
Abbildung 2b: Dreidimensionale farbcodierte Darstellung der linken kleinen Herzkammer mit den 4 Lungenvenen. Die roten Punkte zeigen die Ablationspunkte, mit denen die Lungenvenenmündungen kreisförmig isoliert werden.
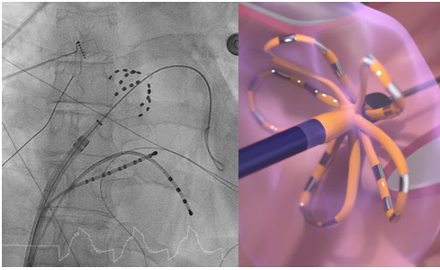
Abbildung 3: Links: zeigt einen PFA-Ablations-Katheter in der Röntgendurchleuchtung (oranger Pfeil), blauer Kreis: Diagnostikkatheter im Sinus coronarius (Herzvene), gelber Kreis: Diagnostikkatheter in der rechten Herzkammer, blauer Pfeil: Draht in der rechten oberen Lungenvene.
Rechts: zeigt eine schematische Darstellung des Katheters, wie er sich an die Lungenvene in der sogenannten „Flower-Konfiguration“ anlegt
Um die zur Ablation benötigten Katheter im Herzen platzieren zu können, werden in die Leistenvene mehrere Zugangsschleusen gelegt. Über die große Hohlvene gelangt man dann in den rechten Herzvorhof (Abb. 1). Um die Verödungslinie um die Lungenvenen im linken Vorhof zu ziehen, muss zunächst durch die Scheidewand der beiden Vorhöfe punktiert werden, um Schleusen und Katheter dort zum Einsatz bringen zu können. Große Aufmerksamkeit schenkt man während der Ablation auch nahe gelegenen Strukturen, wie Speiseröhre, Zwerchfellnerv und Herzkranzgefäßen, welche bei der Verödung unbedingt geschont werden sollen.
Häufig wird mittels moderner dreidimensionaler Magnetfeld-basierender Methoden eine „Landkarte“ des Herzens erstellt, um danach in Echtzeit im dreidimensionalen Raum den Eingriff durchführen zu können, wie die Abb 2b zeigt.
Aufwand aus Sicht des Patienten
Die Katheterablation von Vorhofflimmern dauert zwischen 60 und 90 Minuten und wird in Sedierung, aber meist ohne Vollnarkose durchgeführt. Nach dem Eingriff muss für einige Stunden Bettruhe eingehalten werden, um eine Nachblutung in der Leiste zu verhindern. Auch in den folgenden 2 Wochen sollte man sich körperlich schonen und schweres Heben sowie starkes Beugen in der Leiste vermeiden. Verläuft der Eingriff komplikationslos, ist eine Entlassung am Folgetag möglich. Eine medikamentöse orale Antikoagulation („Blutverdünner“) zur Vorbeugung eines Schlaganfalles muss entsprechend dem Risikoprofil der einzelnen Patientin und des einzelnen Patienten für 3 Monate oder lebenslang eingenommen werden. Um langfristig frei von Vorhofflimmern zu bleiben, ist es wichtig, alle Risikofaktoren und begünstigenden Erkrankungen (Übergewichtigkeit, Bewegungsmangel, Bluthochdruck, Rauchen, Stress, Alkoholkonsum…) zu minimieren. Dazu empfiehlt es sich weiterhin regelmäßige Kontrollen bei einer niedergelassenen Internistin oder Internisten oder Kardiolog:innen wahrzunehmen. Mittels einer ambulanten Rehabilitation lässt sich die Langzeiterfolgsrate des Eingriffes ebenfalls steigern.